▼講演会バックナンバー
2026-01-29
エネルギーの本質と、そのかたち
2026-01-28
冬の見えない殺し屋 ― 室内の二酸化炭素濃度 ―
2026-01-21
市民公開講座
2026-01-19
有機主食 ― 健康の土台は「食」にあり ―
2026-01-16
過去は変えられるのでしょうか
2026-01-15
新年初施療の楽しさ
2026-01-13
男女の健康意識の差
――中医学・生命哲学の視点から――
2026-01-12
再論「治病」と「治未病」
2026-01-11
中国医学は、過去と未来をつなぐ通路
2026-01-03
第4回 腫瘍統合治療学術研討会発表
2025-12-26
中国語による腫瘍統合治療 学術発表会のご案内
2025-12-24
中医学の先進性
2025-12-23
睡眠と免疫
2025-12-22
勉強になる学会
2025-12-21
腸内細菌に関する新たな知見
過去ブログはこちらから
水素を勉強しよう①水素の基礎と発見
カテゴリー 講演会
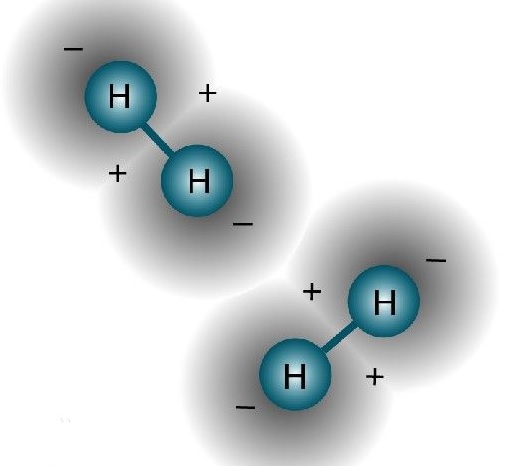
水素は原子番号1番。最もシンプルな構造をもつ元素「水素」は、宇宙で最初に生まれた元素でもあります。その長い歴史に比べ、人類が水素を知ったのはわずか250年前のことです。以来、、私たちは様々な場面で活用する水素を発見し、新たな利用法を生み出してきました。未来へつながる水素の可能性を、一緒に探しにいきましょう。
1766年、イギリスの化学・物理学者、ヘンリー・キャヴェンディッシュ(Henry Cavendish, 1731年10月10日 – 1810年2月24日)は金属と強酸の反応で、燃える気体「水素」が発生することを発見しました。205年前の話でした。電気火花を使った水素と酸素の反応により水が生成することを発見し、水が化合物であることを示したのもヘンリー・キャヴェンディッシュでした。
水素の原子の構造
水素は陽子1個と電子1個からできている。
重さは、1.008 g / (6.02 x 1023) = 1.67 x 10-24 g
水素の原子核(陽子)の直径は、10-15 m~ 10-14 m
電子を含む水素原子(H0)の半径は、約0.1 x 10-9 m= 0.1 nm(ナノメートル) ただし、ボーア(Bohr)の水素原子モデルでは、半径は0.053 x 10-9 m= 0.053 nm 。電子の広がりを持つので、水素原子の直径の決め方にはいろいろある。
電子を2個もつ水素化物イオン(H-)の半径は、約0.2 x 10-9 m。2個の電子同士の反発のため、半径が大きくなる。
H0とH+の電子の広がり(原子核を原点とした分布)を見ると、1個目の電子の広がりはほとんど同じだが、2個目の電子の分布が大きく広がっていることがわかる。
水素の同位体
原子核を構成する陽子の数が同じだが、中性子の数が異なる各種を同位体と呼ぶ。
水素の場合には、中性子が0個の軽水素(H、プロチウム)、中性子が1個の重水素(2H/D、デュウテリウム)、中性子が3個の3重水素(3H/T、トリチウム)の3つの同位体が存在する。(いずれも、陽子は1個、電子は1個)。
水素の同位体としてみなされるものとして、電子と陽電子からなるポジトロニウム、電子をミュオンからなるミュオニウムがある。軽水素に対する質量は、ポジトロニウムが920分の1、ミュオニウムが9分の1である。
「新・元素と周期律」井口洋夫、井口眞 裳華房
文部科学省科学技術週間(一家に1枚)より
1766年、イギリスの化学・物理学者、ヘンリー・キャヴェンディッシュ(Henry Cavendish, 1731年10月10日 – 1810年2月24日)は金属と強酸の反応で、燃える気体「水素」が発生することを発見しました。205年前の話でした。電気火花を使った水素と酸素の反応により水が生成することを発見し、水が化合物であることを示したのもヘンリー・キャヴェンディッシュでした。
水素の原子の構造
水素は陽子1個と電子1個からできている。
重さは、1.008 g / (6.02 x 1023) = 1.67 x 10-24 g
水素の原子核(陽子)の直径は、10-15 m~ 10-14 m
電子を含む水素原子(H0)の半径は、約0.1 x 10-9 m= 0.1 nm(ナノメートル) ただし、ボーア(Bohr)の水素原子モデルでは、半径は0.053 x 10-9 m= 0.053 nm 。電子の広がりを持つので、水素原子の直径の決め方にはいろいろある。
電子を2個もつ水素化物イオン(H-)の半径は、約0.2 x 10-9 m。2個の電子同士の反発のため、半径が大きくなる。
H0とH+の電子の広がり(原子核を原点とした分布)を見ると、1個目の電子の広がりはほとんど同じだが、2個目の電子の分布が大きく広がっていることがわかる。
水素の同位体
原子核を構成する陽子の数が同じだが、中性子の数が異なる各種を同位体と呼ぶ。
水素の場合には、中性子が0個の軽水素(H、プロチウム)、中性子が1個の重水素(2H/D、デュウテリウム)、中性子が3個の3重水素(3H/T、トリチウム)の3つの同位体が存在する。(いずれも、陽子は1個、電子は1個)。
水素の同位体としてみなされるものとして、電子と陽電子からなるポジトロニウム、電子をミュオンからなるミュオニウムがある。軽水素に対する質量は、ポジトロニウムが920分の1、ミュオニウムが9分の1である。
「新・元素と周期律」井口洋夫、井口眞 裳華房
文部科学省科学技術週間(一家に1枚)より
2019-03-20




